O que é anisaquíase?
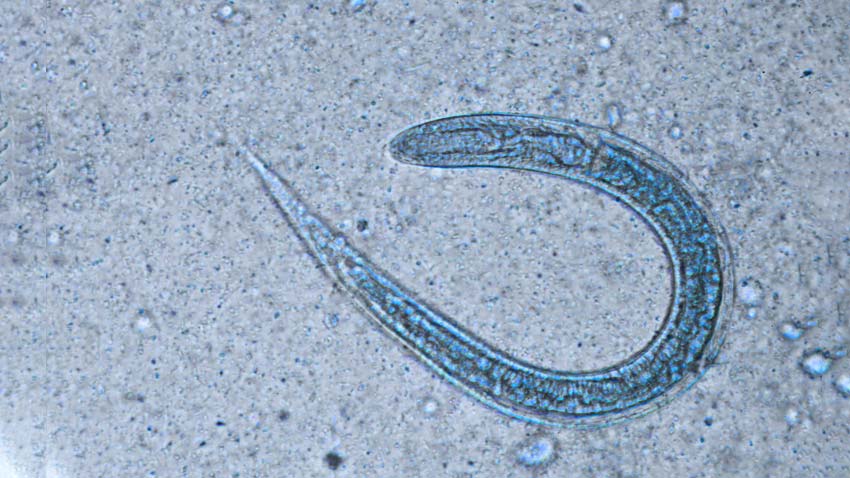
A anisaquíase é uma parasitose intestinal provocada por vermes nemátodes da família Anisakinae, nomeadamente Anisakis simplex, Anisakis physeteris e Pseudoterranova decipiens, que habitualmente adquiridos após a ingestão de frutos-do-mar ou peixes crus.
A anisaquíase ainda é uma doença rara, mas que, devido à crescente popularização dos pratos à base de peixes crus ou mal cozidos, tais como sushis, carpaccios de salmão, salmão defumado ou ceviches, tem vindo a se tornar cada vez mais descrita.
A infecção é uma parasitose típica dos mamíferos marinhos, como baleias, golfinhos, leões marinhos e focas, sendo o homem apenas um hospedeiro acidental. A anisaquíase comporta-se nos animais marinhos de forma semelhante à ascaridíase no homem.
Para entendermos como se dá a contaminação dos seres humanos, precisamos conhecer o ciclo de vida do parasito. São habitualmente seis fases:
- Mamíferos marítimos contaminados eliminam ovos do verme pelas fezes.
- Na água do mar, os ovos chocam e as larvas são liberadas, passando a nadar livremente.
- Essas larvas são ingeridas por crustáceos e começam a se desenvolver no seu interior.
- Quando os crustáceos contaminados são comidos por peixes ou lulas, a larva do verme desloca-se do trato gastrointestinal para os músculos.
- Peixes contaminados são comidos por mamíferos marinhos.
- A larva, agora no seu hospedeiro definitivo, desenvolve-se, vira verme adulto e passa a liberar ovos no intestino desses mamíferos, dando início a um novo ciclo.
A contaminação dos seres humanos se dá por acidente na 5ª fase. Porém, ao contrário do que ocorre nos mamíferos marinhos, a larva do Anisakis não consegue evoluir para verme adulto nos seres humanos.
Quando um humano se contamina, o ciclo de reprodução do parasito é interrompido, pois ele não consegue sobreviver fora do seu hospedeiro habitual.
Portanto, não existe transmissão de ser humano para ser humano, e as pessoas contaminadas não eliminam ovos nem parasitos pelas fezes.
Contaminação dos seres humanos pelo Anisakis
Como já mencionado, o homem contamina-se com o parasito Anisakis quando ingere carne crua ou malpassada de peixes contaminados. Salmão, arenque, cavala e lula costumam transmitir espécies de Anisakis enquanto Alabote e anchova transmitem espécies de Pseudoterranova. O bacalhau pode transmitir ambas espécies.
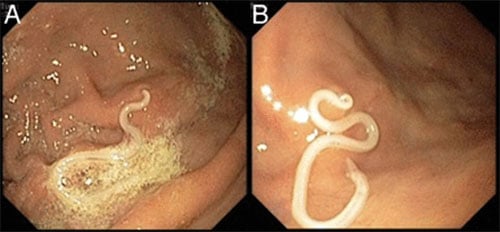
A larva do verme costuma estar alojada no músculo dos peixes, sendo possível sua identificação no momento em que o peixe está sendo fatiado.
As melhores medidas preventivas são a cozedura do peixe a, no mínimo, 70ºC ou congelamento a -20ºC por um período mínimo de 72 horas (idealmente por 7 dias) ou a -35ºC por, pelo menos, 24 horas. O processo de defumação não mata o parasito.
Apesar da recente explosão no número de restaurantes de sushi no mundo ocidental nos últimos anos, a anisaquíase continua sendo pouco comum. Isso ocorre por 3 motivos:
- Restaurantes de qualidade congelam o peixe antes destes serem servidos ao público.
- Muitos restaurantes utilizam peixes criados em cativeiro, sem contato com a vida marinha natural.
- Chefs de sushi devidamente treinados são capazes de detectar as larvas do Anisakis no momento do preparo do peixe.
Em quais países existem casos de anisaquíase?
A anisaquíase é uma verminose ainda bastante desconhecida do público em geral e até da classe médica. Todavia, com a crescente popularização dos restaurantes que servem peixe cru, principalmente ceviche e sushi, os casos de infecção pelo Anisakis começaram a ser descritos com cada vez mais frequência.
No Japão, país com maior incidência dessa verminose, a taxa anual de infecção é de 3 casos novos para cada 1 milhão de habitantes. Isso significa, aproximadamente, 400 novos casos por ano.
Na Holanda, país no qual há o hábito de comer arenque cru (haring), essa parasitose também é relativamente conhecida. Aliás, o primeiro caso de anisaquíase descrito na literatura médica veio exatamente da Holanda, em 1960.
Atualmente, porém, devido a uma lei que obriga o congelamento do haring por 7 dias antes da comercialização ao público, a doença praticamente desapareceu.
Nos restantes dos países ocidentais, a incidência da anisaquíase é desconhecida. É muito provável que a real incidência dessa verminose seja maior que aquela efetivamente notificada. No Brasil, por exemplo, não há casos registrados de anisaquíase. Entretanto, o verme já foi encontrado pela vigilância sanitária em diversos tipos de peixes, tais como anchova, bacalhau, cavala, dourado, peixe-espada e vieiras. É possível que as pessoas estejam se infectando com o verme, mas o diagnóstico não esteja sendo feito.
Em Portugal, houve recentemente grande divulgação nas mídias sociais do caso de um paciente de 32 anos que deu entrada no serviço de urgências com intensa dor abdominal, vômitos e febre após ter comido sushi.
Sintomas
A maioria dos sintomas associados à anisaquíase são devidos a danos diretos aos tecidos do trato gastrointestinal ou à reação alérgica provocada pelo parasito.
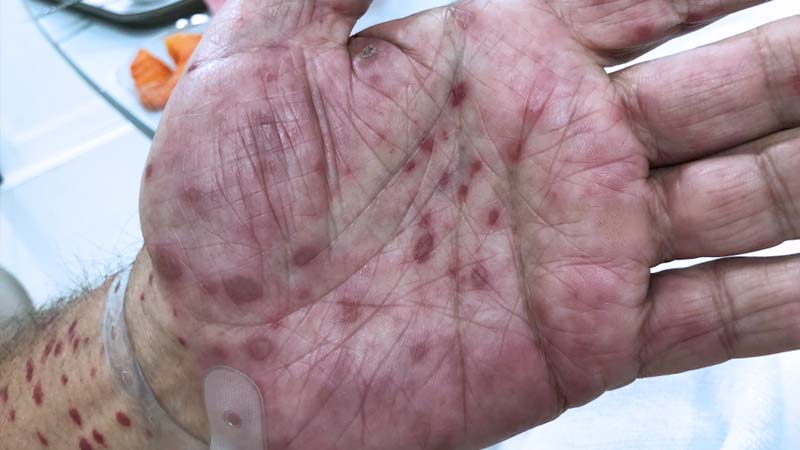
A reação alérgica, que é a forma menos comum, surge rapidamente após a ingestão do peixe cru infectado. Alguns indivíduos desenvolvem rash na pele, coceira e formigamento na garganta. Casos de angioedema e anafilaxia são raros, mas já foram descritos.
O quadro é parecido com o de qualquer alergia alimentar, não sendo improvável que alguns dos casos sejam confundidos com alergia a frutos-do-mar. Casos de alergia podem ocorrer mesmo se o peixe tiver sido devidamente cozinhado e a larva estiver morta.
Os sintomas gastrointestinais costumam surgir devido a uma reação inflamatória provocada pela presença do parasito. Habitualmente, a larva tenta penetrar a mucosa do sistema digestivo e acaba morrendo no meio do caminho. A presença do verme morto estimula uma intensa reação inflamatória, que pode provocar uma massa ou abscesso no esôfago, estômago ou intestinos.
A anisaquíase gástrica geralmente surge entre 1 a 8 horas após a ingestão do peixe contaminado e caracteriza-se por dor estomacal aguda, febre baixa, náuseas e vômitos.
Os pacientes que apresentam vômitos podem eliminar a larva desta forma, acabando por ficarem curados.
Já a anisaquíase intestinal costuma desenvolver-se de 5 a 7 dias após a ingestão da larva e pode estar associada a dor abdominal intensa, distensão abdominal, febre e obstrução intestinal pela massa inflamatória. Diarreia com sangue ou muco também são manifestações comuns.
A larva costuma ficar no intestino delgado e raramente chega ao intestino grosso. Eventualmente, a larva consegue perfurar o intestino, caindo na cavidade peritonial e provocando um quadro de peritonite.
Diagnóstico
Na maioria dos casos, o diagnóstico da anisaquíase é feito através da endoscopia digestiva alta, que é capaz de visualizar facilmente a larva do verme dentro do estômago (leia: Endoscopia digestiva alta).
Quando o verme já não se encontra mais no estômago, o diagnóstico torna-se mais difícil. Existem exames de sangue capazes de detectar a infecção pelo Anisakis, mas eles não estão disponíveis em todos os laboratórios e é preciso um elevado grau de suspeição por parte do médico para solicitar estas análises. Se o médico nunca viu um caso de anisaquíase, provavelmente não irá passar pela sua cabeça pesquisar essa parasitose.
Tratamento
Quando o verme encontra-se no estômago, a sua remoção através da endoscopia digestiva é suficiente para curar o paciente. Os sintomas desaparecem logo ao final do procedimento.
Quando o verme já não se encontra mais no estômago e penetrou a mucosa do intestino, provocando abscesso ou obstrução intestinal, a cirurgia é forma mais indicada de tratar a infecção.
Casos de sucesso com o tratamento à base de albendazol 400 mg de 12/12 horas por 3 dias têm sido descritos.
Referências
- Miscellaneous nematodes – UpToDate.
- Anisakis – Autoridade de Segurança Alimentar e Económica (Portugal).
- Parasites – Anisakiasis – Centers for Disease Control and Prevention.
- Anisakidosis: Perils of the deep – Clinical infectious diseases : an official publication of the Infectious Diseases Society of America.
- Treatment of anisakiasis with albendazole – The Lancet.
- Sushi delights and parasites: the risk of fishborne and foodborne parasitic zoonoses in Asia – Clinical infectious diseases : an official publication of the Infectious Diseases Society of America.
- Guerrant RL, Walker DH, Weller PF (eds). Tropical Infectious Diseases: Principles, Pathogens, and Practice, 2nd Edition. Philadelphia 2006. pp 1236-1237.
Autor(es)
Médico graduado pela Universidade Federal do Rio de Janeiro (UFRJ), com títulos de especialista em Medicina Interna e Nefrologia pela Universidade Estadual do Rio de Janeiro (UERJ), Sociedade Brasileira de Nefrologia (SBN), Universidade do Porto e pelo Colégio de Especialidade de Nefrologia de Portugal.






Deixe um comentário